来源:原创 关注科研进展的 大米和小米 2023-11-28 19:14 发表于广东
VOL 3139
自闭症的基因疗法迎来一丝新的曙光。
11月27日,在全球首个CRISPR/Cas9 基因编辑疗法在英国有条件上市10天后,中国科学家开发的单碱基编辑技术,也被研究证实能对特定的基因突变导致的自闭症症状,起到明显的改善作用。
这项研究发表在《Nature》杂志的子刊《Nature Neuroscience》上,上海交通大学医学院松江研究院/中国科学院脑科学与智能技术卓越创新中心(神经科学研究所)仇子龙研究员和复旦大学脑科学转化研究院程田林研究员是论文的共同通讯作者。
“如果自闭症领域也会出现类似英国批准的CRISPR/Cas9 基因编辑疗法,那我们应该是在努力的团队之一”,仇子龙此前在评价全球首个基因编辑疗法有条件获批时表示。
01
打一针过后,自闭症小鼠的社交障碍逐渐消失了
在这篇名为《Whole-brain in vivo base editing reverses behavioral changes in Mef2c mutant mice》的论文中,仇子龙和程田林团队探索了应用单碱基编辑技术对导致孤独症的基因突变在大脑内进行准确的修复的可能性。
仇子龙之前在与上海交通大学医学院附属新华医院的合作研究中,在一个自闭症儿童身上发现了一个新发的单核苷酸变异(SNVs),该变异是在MEF2C 基因中发现,表现为在基因片段上一个特定的点位上(c.104T>C, p.L35P),本应该是胸腺嘧啶(Thymine)的碱基,变成了胞嘧啶(Cytosine)。
MEF2C基因已被证实是一个很重要的孤独症风险基因,突变会导致神经发育迟滞等症状,但是该新发点突变对于MEF2C基因功能的影响未知。该团队首先用分子细胞生物学的方法证实了L35P点突变会导致MEF2C蛋白的表达水平显著降低。
然后,应用CRISPR-Cas9介导将Mef2c L35P 点突变敲入小鼠模型后,发现Mef2c L35P 杂合突变小鼠大脑中存在孤独症相关的神经生理学特征,伴随有相关的发育异常现象,并且表现出社交障碍以及刻板行为等孤独症核心症状。
为了修复这个孤独症小鼠大脑中的单点基因突变,仇子龙和程田林构建了一个新型的基于CRISPR/Cas9 的胞嘧啶碱基编辑系统(CBE),并将它命名为“AeCBE”,它的作用是把能够将前述基因点位上异常的胞嘧啶(C)转换为正常的胸腺嘧啶(T)。
但要把这个碱基编辑系统送进小鼠的体内,还需要跨越血脑屏障(BBB,脑组织的毛细血管内皮细胞间的紧密连接,可有效地阻挡蛋白质从血液进入脑组织,也能减慢小分子物质的通过)。为此,该团队又设计了一种特定血清型的腺相关病毒载体(AAV-PHP.eB),将AeCBE包装进进该载体后,可成功跨越BBB。
最后,该团队通过在小鼠尾巴的静脉上注射的方式,将包含有AeCBE的AAV注射进小鼠体内。
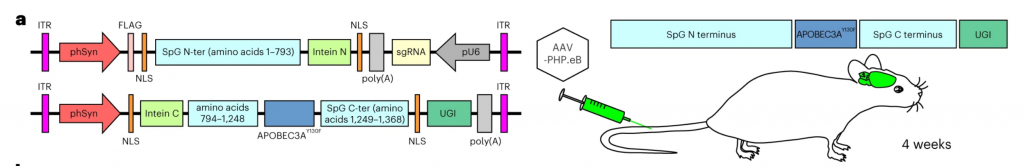
AAV-PHP.eB及其注射和表达示意图
几个星期后,研究团队对碱基编辑系统在小鼠大脑内是否起到预期作用进行了检测。结果发现,正确编辑的基因片段,在小鼠大脑的多个脑区得到表达,单一碱基的突变得到有效的修复。
随后进行的神经生理学变化以及行为学表型结果表明,Mef2c L35P突变杂合小鼠大脑中降低的Mef2c蛋白表达水平得到恢复,并且其社交障碍以及重复刻板性行为也得到了明显的改善。
02
碱基编辑技术未来在脑遗传病中或能派上大用场
仇子龙和程田林团队的文章发表后,国内多位专家对这项研究进行了点评。
华东师范大学李大力教授表示,相比基于CRISPR的同源重组修复(HDR)技术的各种限制,同样基于CRISPR的衍生技术——碱基编辑器(BE)已成为广受欢迎的碱基高效替换工具。
因无需依赖外源模板和DNA双链断裂(DSB),理论上也不依赖于细胞分裂,碱基编辑技术已广泛应用于生命科学的众多领域,特别是基于血红蛋白病、早衰症、视网膜病变、神经肌肉病、心肌病、耳聋等疾病的基因治疗。
李大力说,人类致病性遗传突变中有近6成为点突变,遗传变异也是导致多种神经系统疾病发生的关键因素。考虑到神经元在出生后很快失去分裂能力的特点,BE较HDR在神经系统疾病治疗中更具有应用的潜力和可行性,但BE是否真能用于逆转大脑的致病突变而治疗神经发育障碍疾病(如自闭症),目前尚未有相关报道。
仇子龙等人的论文创新性开发出高效且更少旁观者突变的AeCBE系统,最终通过在体全脑碱基编辑首次实现了自闭症小鼠的有效治疗。李大力认为,该研究为自闭症治疗提供了新的思路,并进一步表明了碱基编辑技术治疗遗传性脑部疾病的巨大潜力。
北京大学魏文胜教授则认为,仇子龙等人的研究,在“概念上证明了碱基编辑器可以通过一次给药的方式,对脑部遗传疾病进行精准且有效的基因治疗,为未来ASD及相关遗传疾病治疗提供了良好的思路与范式”。
魏文胜还乐观的认为,针对治病位点的多样性,未来不仅是CBE,ABE编辑系统以及近期报道的多个基于ABE系统TadA脱氨酶进化得到的新型CBE、CGBE、ACBE等碱基编辑工具均有望在遗传疾病的治疗中得到应用。(A=腺嘌呤,G=鸟嘌呤)
上海科技大学的朱俊杰博士和陈佳研究员则表示,“虽然ASD的成因极其复杂,但这项研究证明了体内碱基编辑在神经发育障碍治疗中的潜力,同时也为其他类型的碱基编辑器在脑内递送以及编辑带来了新的启发”。
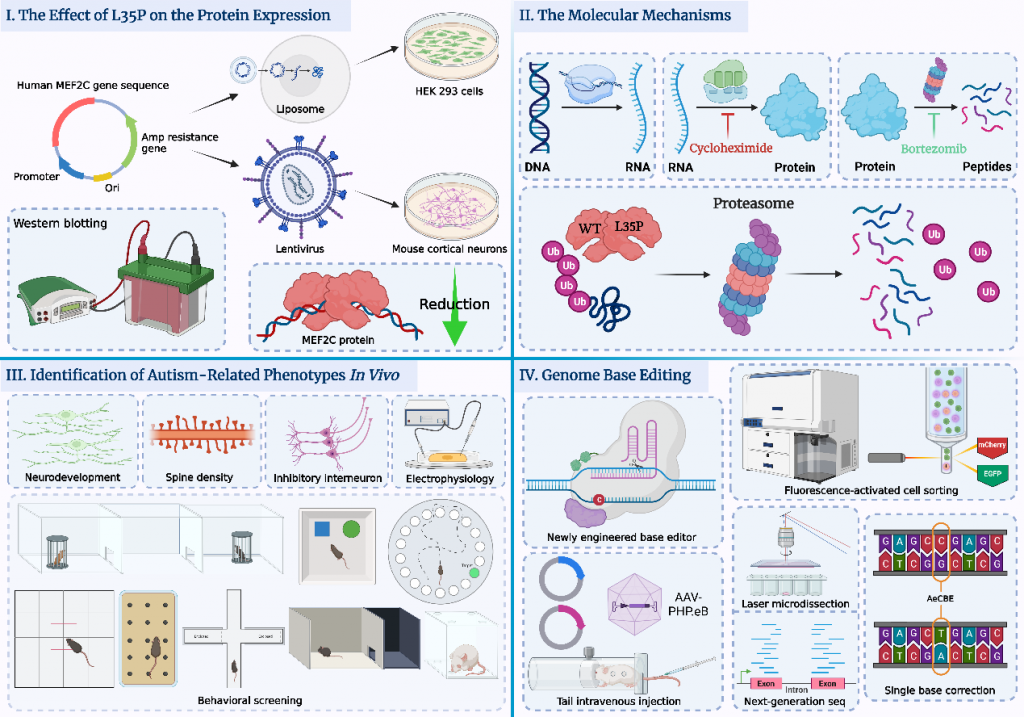
图I: L35P点突变显著降低MEF2C蛋白表达水平。图II: L35P点突变通过泛素化蛋白酶体降解途径介导MEF2C蛋白翻译后快速降解。图III: Mef2c L35P杂合小鼠表现出与孤独症相关的异常神经发育,突触密度降低,抑制性中间神经元数量下降及异常的电生理表型,且出现孤独症相关的行为学表型。图IV: 基于CRISPR/Cas9系统开发的新型胞嘧啶单碱基编辑系统,通过体内及体外验证了其在目标靶点的碱基编辑效率以及脱靶事件,证明该系统是高效,准确且安全的。
03
自闭症的未来不能仅靠基因治疗
虽然仇子龙等人在小鼠模型中,针对特定新发基因突变导致的自闭症症状进行脑内碱基编辑,实现了核心症状的减退,为自闭症的基因治疗带来了新的希望,但自闭症要实现基因治疗还任重道远。
中山大学附属第三医院邹小兵教授也肯定了仇子龙和程田林团队这项工作对于自闭症康复的意义,“哪怕是在特定的单核苷酸变异中找到了有效的基因治疗手段,那至少对因为这个基因导致的自闭症人群而言,也是非常有价值的一件事情”。
但自闭症的复杂性也在于,与自闭症相关的基因突变已发现了数百个,有的是单核苷酸变异(SNVs),有的是拷贝数变异(CNVs)。邹小兵说,好比一本书,如果一本书里的一个字印错了,导致表达的意思错误,这个叫做单核苷酸变异;如果是书里的某一段话被重复印了很多遍,这种是拷贝数变异。
单核苷酸变异的修复相对比较简单,只需要把错了的那个字改成正确的就行。而拷贝数变异的修复就会很复杂,你得看从哪开始复制错了,是多了还是少了,重复的次数有多少,要把哪些错误的段落恢复成正确的样子——这比改错字的难度大多了。
邹小兵说,如果不是确定的因为某个基因的单核苷酸变异导致孩子出现自闭症症状,现阶段关注自闭症的基因治疗还比较遥远。“针对孩子的具体情况,持续做科学的有针对性的、个性化的干预和训练,还是目前应对自闭症的主要方式”。
相关阅读:
最新:中国人独有的9个自闭症基因被发现,有望治疗?
自闭症新突破!一种基因疗法对小鼠有效,中国科学家正试验猴子
他曾制造出“自闭猴”,现在又有新进展:自闭症即将可以通过基因被诊断了?!
文 | 谭万能
编辑 | 若水 眉沙
封面图 |Pexels
